Актуальность. В настоящее время применение стабилизирующих конструкций в хирургическом лечении заболеваний позвоночника различной этиологии стало рутинным. Для формирования спондилодеза позвоночных сегментов используются винты для транспедикулярной стабилизации, межтеловые импланты, устанавливаемые из заднего, трансфораминального и переднего доступов. Интраоперационная точность установки имплантов контролируется с помощью электронно-оптического преобразователя (ЭОП). Несмотря на это, по данным литературы, частота ошибок, связанных с неправильным расположением имплантов при дегенеративных заболеваниях доходит до 4.2%, а при коррекции сколиотических деформаций – до 25% [1,2,3,9]. В этих случаях могут возникать неврологические, сосудистые осложнения, а также повреждения твердой мозговой оболочки [4,5]. В ряде случаев, особенно при сколиотических деформациях, установка имплантов затруднена из-за анатомических особенностей позвоночных сегментов, что влечет за собой необходимость проведения большего количества рентгеновских снимков во время операции. В результате возрастает величина лучевой нагрузки, как на пациента, так и на оперирующих хирургов. Повышение безопасности пациента является сегодня одной из приоритетных задач практической медицины. Последние разработки в сотрудничестве со специалистами технических дисциплин позволяют сегодня говорить о формировании целого направления, в основе которого лежит интраоперационное использование роботов, осуществляющих типовые манипуляции или роботоассистенции [6,7,8,12].
В хирургическом лечении заболеваний позвоночника, требующих стабилизации позвоночных сегментов, в стадии внедрения находится метод роботоассистенции. Его принцип заключается в том, что робот-ассистент самостоятельно располагает инструмент для введения импланта (винта) таким образом, чтобы точка введения, траектория и глубина погружения были идентичны виртуально запланированным по данным компьютерной томографии в 3D изображениях.
Цель исследования: оценить применение метода роботоассистенции в хирургическом лечении дегенеративных заболеваний пояснично-крестцового отдела позвоночника.
Материалы и методы. С августа по декабрь 2009 года в отделении спинальной нейрохирургии НИИ Нейрохирургии им. акад. Н.Н.Бурденко РАМН было выполнено 37 хирургических вмешательств пациентам с дегенеративными заболеваниями пояснично-крестцового отдела позвоночника. В 16 случаях впервые в России стабилизирующий этап осуществлялся с использованием роботоассистенции (SpineAssist; MAZOR Surgical Technologies, Caesarea, Israel). Распределение пациентов по видам стабилизирующих операций представлено в табл. 1.
| Вид стабилизирующей операции | С роботоассистенцией | Без роботоассистенции |
| Транспедикулярная стабилизация одного сегмента позвоночника | 3 | 4 |
| Транспедикулярная стабилизация с установкой межтелового импланта одного сегмента позвоночника | 5 | 11 |
| Транспедикулярная стабилизация двух и более сегментов позвоночника | 3 | 6 |
| Билатеральная косая транскорпоральная чресдисковая стабилизация «GO-LIF» | 5 | Установка невозможна |
| Итого: | 16 | 21 |
В исследуемую группу вошли пациенты со стенозами позвоночного канала, нестабильностью позвоночных сегментов, синдромом оперированного позвоночника, спондилолистезами I, II степени.
Предоперационное обследование пациентов включало в себя неврологический осмотр, обзорную спондилографию (функциональные спондиограммы при наличии признаков нестабильности), КТ и МРТ-исследования. В случаях, когда планировалось применить метод роботоассистенции «SpineAssist», компьютерная томография выполнялась по следующему протоколу:
- срезы должны быть представлены в одной серии
- сканирование в спиральном режиме с углом наклона трубки 0
- поле зрения (FOV) 200 мм (максимум 250 мм)
- матрица 512 и выше
- толщина среза не более 1 мм
- коллимация 6х0.75
- питч 0.4
- значение напряжения/экспозиция 140 кВ/200 мАс
- фильтр реконструкции «bone» (в томографах Philips соответствует «D»)
Оценка эффективности хирургического лечения осуществлялась с помощью разработанной в Институте шкалы. Для оценки клинических исходов также использовались модифицированные классы исходов Kawabata et al [10,11].
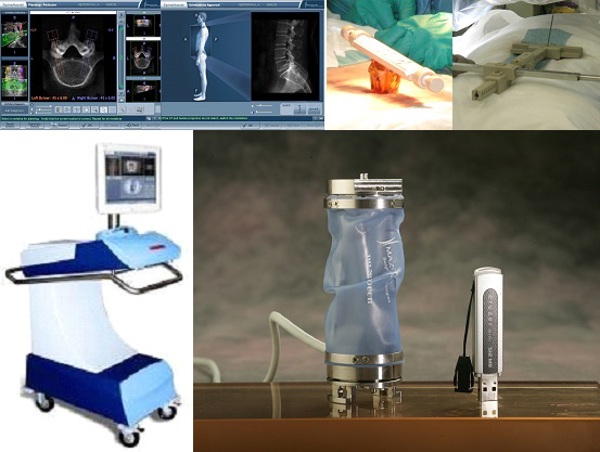
Система роботоассистенции «SpineAssist» (Рис.1) состоит из 4-х компонентов: программа предоперационного планирования (А), рабочая станция (Б), платформы для крепления на позвоночнике (В), робот – позиционирующее устройство (Г).
Для использования метода роботоассистенции ключевым является КТ-исследование. В данном случае результаты КТ, помимо традиционной информативности, необходимы для проведения предоперационного планирования – виртуального проведения имплантов с помощью графического интерфейса на рабочей станции «SpineAssist» или на персональном компьютере хирурга. Как правило, данная манипуляция выполняется накануне операции.
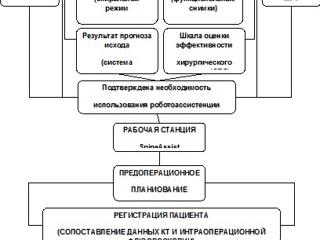
На схеме 1 представлен алгоритм применения метода роботоассистенции.
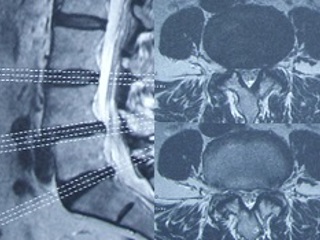
В операционной в положении пациента лежа на животе в условиях эндотрахеального наркоза с помощью ЭОП проводится регистрация позвоночного сегмента и синхронизация данных предоперационного КТ-исследования с реальной рентгенографической картиной. (Рис. 2).
Рис. 2. Синхронизация предварительных (дооперационных) рентгенологических данных и интраоперационного исследования: А – этап I регистрации ЭОП (снимок в передне-задней проекции); Б – этап II регистрации ЭОП (косой снимок); В – этап III регистрации – снимки получены на рабочей станции; Г – этап IV регистрации - совмещение предоперационных КТ с данными рентенографических снимков; Д – этап V - завершение регистрации.
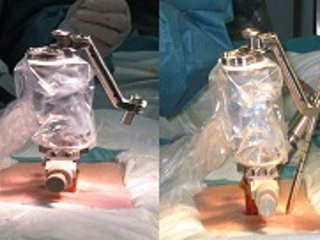
Во время операции, после завершения этапа регистрации, помещенный в стерильный герметичный пакет робот (Рис. 3) устанавливается на платформе (А). Полученная конструкция отличается жесткостью и неподвижностью относительно позвоночника пациента. К роботу фиксируется «рука», которая определяет траекторию введения импланта (Б). Затем хирург выбирает позвонок и имплант для введения, учитывая диаметр и длину (мм) последнего, после чего робот самостоятельно позиционирует направляющую «руку» согласно запланированной траектории (В).
Следующим этапом с помощью тубулярного ранорасширителя формируется канал для дрели, метчика или отвертки с винтом. (Г). Последовательность установки винтов определяется хирургом.
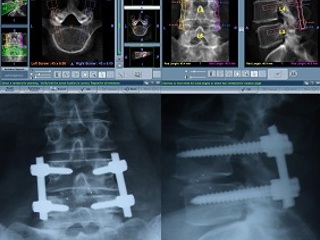
В качестве клинического примера приводим случай установки 4-х винтовой системы с межтеловым имплантом с применением метода роботоассистенции у пациентки Н., 59 лет с нестабильностью сегмента L4-L5, спондилолистезом I степени (Рис 4).
При поступлении выявлена III степень выраженности дегенеративного поражения (52%) по шкале Института.
Произведено оперативное лечение – декомпрессия на уровне L4-L5, установка межтелового импланта, транспедикулярная стабилизация указанного сегмента с применением метода роботоассистенции «SpineAssist» (Рис. 5).
Пациентка активизирована в первые сутки после операции. В неврологическом статусе отмечен регресс болевого синдрома в ногах. При выписке выявлена I степень выраженности дегенеративного заболевания (11%) по шкале Института, I класс исхода по Kawabata et al (отсутствие боли и неврологических нарушений).
Возможность точного проведения винтов с помощью метода роботоассистенции повлекло за собой появление новых видов стабилизации позвоночных сегментов. Предоперационное планирование на основании анализа большого количества (до 600) аксиальных срезов компьютерной томографии и реконструкций в сагиттальной проекции. Моделирование стабилизирующего этапа на компьютере хирурга реализованы в системе билатеральной транскорпоральной стабилизации сегмента пояснично-крестцового отдела позвоночника «GO-LIF» (Guided Oblique Lumbar Interbody Fusion).
К преимуществам системы относятся:
- отсутствие травмы фасеточных суставов
- возможность сочетания с существующими методиками межтелового спондилодеза (PLIF, TLIF, ALIF).
В качестве клинического примера приводим случай применения метода роботоассистенции при установке системы транскутанной стабилизации «GO-LIF».
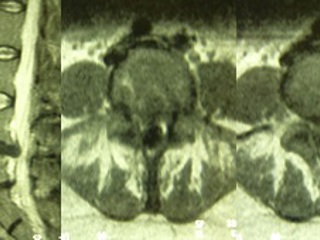
Пациентка П., 43 лет с диагнозом «Секвестрированная грыжа диска на уровне L4-L5 справа, нестабильность в сегменте L4-L5». Из анамнеза известно, что манифестация заболевания с приступов люмбалгии около 5 лет назад. С 2009 года стали беспокоить интенсивные боли в пояснично-крестцовом отделе позвоночника при изменении положения тела, при ходьбе с иррадиацией по задней поверхности правой ноги. Консервативное лечение без эффекта. При поступлении была выявлена III степень выраженности дегенеративного поражения (45%) по шкале, указывающая на целесообразность проведения хирургического лечения (Рис. 6).
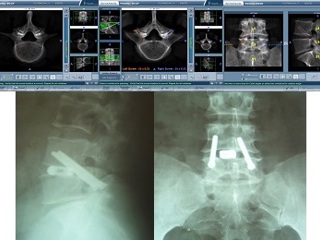
Произведено оперативное лечение - билатеральная транскорпоральная стабилизация сегмента L4-L5 системой «GO-LIF», микродекомпрессия на уровне L4-L5 справа, межтеловая стабилизация сегмента L4-L5 кейджем (Рис. 7).
Пациентка активизирована в первые сутки после операции. При выписке болевой синдром в пояснично-крестцовом отделе позвоночника и правой ноге, имевший место до операции, регрессировал (оценка по шкале Института), выявлена I степень выраженности дегенеративного заболевания (10%) и I класс исхода по Kawabata et al. (отсутствие боли и неврологических нарушений).
Результаты.
Проведен сравнительный анализ основных характеристик стабилизирующего этапа стандартной операции и стабилизации с использованием метода роботоассистенции для четырех-винтовой системы. В ходе работы осуществлялся мониторинг длительности стабилизирующих этапов, величины лучевой нагрузки и точность установки импланта. Последняя оценивалась нейрорадиологом на основании анализа спондилограмм и КТ-исследований с 3D реконструкцией. Результаты сравнения представлены в табл. 2.
| Критерии для сравнения стабилизирующего этапа операции | Без применения метода роботоассистенции | С применением метода роботоассистенции |
| Длительность установки одного винта в среднем и конструкции (мин.) | 7 мин/28мин | 15 мин/45мин. |
| Величина лучевой нагрузки при установке одного винта /всей системы (количество снимков) | 6/26 | 2/4 |
| Точность установки винта (мм) | 3-4,5мм | 1-1,5мм |
Длительность установки конструкции оценивалась из расчета времени, необходимого для установки одного винта и четырехвинтовой системы в минутах. Длительность стабилизирующего этапа операции с использованием метода роботоассистенции оказалась выше при первых двух операциях. Это естественно связано с тем, что метод находится на стадии апробации. Однако в остальных случаях была отмечена тенденция к уменьшению длительности стабилизирующего этапа. Важно отметить, что в случаях отсутствия четких анатомических ориентиров в операционной ране, введение винтов с помощью роботоассистенции значительно сокращает время установки винта. Рентгенологический контроль выполнялся на всех этапах при выполнении первых трех операций. В остальных случаях рентгеновские снимки проводились только для регистрации робота в операционной ране и для контроля положения имплантов после их установки. Точность установки имплантов оценивалась на основании анализа КТ-исследования с 3D реконструкцией. Пациент, которому планировалось выполнить стандартный стабилизирующий этап, проходил обследование по КТ – протоколу, необходимому для использования метода роботоассистенции. Далее, на рабочей станции составлялся виртуальный план операции, который сравнивался с контрольными КТ – исследованиями после операции.
Если пациенту во время операции стабилизация выполнялась стандартным (без использования робота) методом, контрольное КТ-исследование для оценки точности проведения винтов выполнялось перед выпиской.
Для оценки точности установки имплантов нами измерялось отклонение у головки и конца винта (мм) от запланированной траектории. Для винтов, установленных без использования метода роботоассистенции, среднее отклонение составило 2,08-4,9 мм (разброс +/- 2,82 мм). При оценке винтов, установленных с использованием методики роботоассистенции, среднее отклонение от заданной траектории для четырех винтов в переднезадней проекции составило 0,88-0,65 мм (разброс 0+/-1,5 мм), в боковой проекции – 0,81-0,54 мм (разброс 0+/-1,5 мм) и в аксиальной проекции – 1,38-0,17 мм (разброс 1+/-1,5 мм). Среднее отклонение – 1,02-0,56 мм (разброс 0+/-1,5 мм). Таким образом, установлено, что точность проведения винтов при использовании роботоассистенции ограничена пределами 1 мм.
На наш взгляд применение метода роботоассистенции особенно актуально в тех случаях, когда хирургическое лечение проводится в условиях выраженных анатомических особенностей оперируемого позвоночного сегмента (деформация дуг позвонков, ротационная деформация позвонка и.т.д.) и для установки специально разработанных стабилизирующих конструкций. Помимо этого, метод роботоассистенции полезен для молодых хирургов, а также для клиник, где стабилизирующие операции только начинают осваивать.
Выводы.
1. Применение метода роботоассистенции на этапе стабилизации позвоночных сегментов обеспечивает высокую точность установки имплантов и является безопасным для пациента.
2. Интраоперационное использование роботоассистенции увеличивает длительность хирургического вмешательства при стандартных вмешательствах и сокращает длительность стабилизирующего этапа в условиях неблагоприятных анатомических особенностей оперируемого сегмента (истончение корней дуг позвонков, ротационная деформация стабилизируемого сегмента).
3. Использование роботоассистенции снижает величину лучевой нагрузки, как на пациента, так и на оперирующую бригаду.
4. С применением метода роботоассистенции появилась возможность проведения новых видов стабилизации позвоночника (билатеральная косая транспедикулярная межтеловая стабилизация GO-LIF), которые невозможно осуществлять без данной системы или крайне рискованно.
Список литературы:
1. Gaines RW Jr: The use of pedicle-screw internal fixation for the operative treatment of spinal disorders. J Bone Joint Surg Am 82-A:1458–1476, 2000.
2. Gertzbein SD, Robbins SE: Accuracy of pedicular screw placement in vivo. Spine 15:11–14, 1990.
3. Jerosch J, Malms J, Castro WH, Wagner R, Wiesner L: Accuracy of pedicle screws following instrumented dorsal fusion of the lumbar spine [in Ger¬man]. Z Orthop Ihre Grenzgeb 130:479–483, 1992.
4. Esses SI, Sachs BL, Dreyzin V: Complications associated with the technique of pedicle screw fixation: A selected survey of ABS members. Spine 18:2231– 2238, 1993.
5. Brantigan JW, Neidre A, Toohey JS: The Lumbar I/F Cage for posterior lumbar interbody fusion with the variable screw placement system: 10-year results of a Food and Drug Administration clinical trial. Spine J 4:681–688, 2004.
6. Lieberman I. H, M.D., Togawa, M.D., Ph.D., M. Kayanja, M.D., Ph.D., Edward C. Benzel, M.D.: Bone-mounted Miniature Robotic Guidance for Pedicle Screwand Translaminar Facet Screw Placement: Part I – Technical Development and a Test Case Result. Neurosurgery 59:641-650, 2006.
7. Nolte L, Zamorano L, Arm E, Visarius H, Jiang Z, Berlerman U, Schwarzenbach O: Image-guided computer-assisted spine surgery: A pilot study on pedicle screw fixation. Stereotact Funct Neurosurg 66:108–117, 1996.
8. Nolte LP, Zamorano LJ, Jiang Z, Wang Q, Langlotz F, Berlemann U: Image-guided insertion of transpedicular screws: A laboratory set-up. Spine 20: 497–500, 1995.
9. Slomczykowski M, Roberto M, Schneeberger P, Ozdoba C, Vock P: Radia¬tion dose for pedicle screw insertion: Fluoroscopic method versus computer-assisted surgery. Spine 24:975–982, 1999.
10. Multicriterian assessment of the degenerative lumbar spine diseases. Nazarenko A.G. // Materials of 14 World Congress of Neurological surgery// Boston, USA, 2009.
11. Outcome prognosis for the patients with degenerative lumbar spine diseases Nazarenko A.G.// Materials of 14 World Congress of Neurological surgery // Boston, USA, 2009
12. Berlemann U, Monin D, Arm E, Nolte LP, Ozdoba C: Planning and insertion of pedicle screws with computer assistance. J Spinal Disord 10:117–124, 1997.
Коновалов Н.А., Шевелев И.Н., Корниенко В.Н., Зеленков П.В., Исаев К.А., Асютин Д.С.
Статья опубликована в журнале Вопросы нейрохирургии № 3, 2010, Том 74, стр. 10-15.
7 декабря 2013 г.
Ещё больше полезной информации на нашем Телеграм-канале